Senyawa ionik adalah senyawa yang atom-atomnya berikatan secara ionik. H2O disatukan oleh ikatan kovalen polar.
![]()
Perbedaan Sifat Senyawa Ion Dan Senyawa Kovalen Po
Biasanya sebuah elektron lebih tertarik pada satu atom daripada yang lain membentuk ikatan kovalen polar.

. Phambao_xinh 1 week ago 5 Comments. Senyawa Polar Ikatan kovalen polar adalah ikatan yang pasangan elektron ikatannya cenderung tertarik ke. Senyawa ionik terbentuk oleh transfer elektron yang bermuatan positif dan negatif sedangkan senyawa kovalen terbentuk dengan berbagi elektron.
Bentuk lelehan bersifat konduktor karena susunan antar partikel yang renggang sehingga ion-ion dapat. Definisi Gaya Dipol Permanen. Kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.
Anda dapat memprediksi ikatan kovalen akan terbentuk antara dua atom nonlogam. Sebagai contoh atom-atom dalam air H2O disatukan oleh ikatan kovalen polar. 1Senyawa ion memiliki titik didih dan titik leleh yang tinggi 2.
Pada senyawa ion titik leleh rendah sdangkan pada senyawa kovalen titik leleh tinggi. Senyawa ion tidak dapat menghantarkan listrik ketika dalam keadaan padatan namun bisa menghantarkan listrik jika dilarutkan dalam pelarut polar. Ikatan ion dalam senyawa ionik lebih kuat.
Jika dua atom nonlogam sejenis diatomik membentuk suatu senyawa kovalen misalkan H2 N2 Br2 dan I2 maka ikatan kovalen yang terbentuk memiliki keelektronegatifan yang sama atau tidak memiliki perbedaan. Pada contoh ikatan kovalen polar yaitu pada molekul HCl pasangan elektron ikatan PEI cenderung tertarik ke salah satu atom yang memiliki elektronegativitas lebih besar yaitu atom Cl oleh karena itu bentuk molekulnya mengutub pada atom Cl sehingga menjadi asimetris tidak simetris. Juga senyawa kovalen dapat larut dalam.
Sifat-sifat senyawa kovalen Titik didih dan titik leleh rendah. Perbedaan antara senyawa ion dan senyawa kovalen terletak pada. Sifat-sifat senyawa ion Titik didih dan titik leleh tinggi Mudah larut dalam pelarut polar Pada suhu kamar berbentuk padatan Dalam bentuk larutanlelehan dapat menghantarkan listrik 2.
Senyawa ion juga lebih larut dalam air dibandingkan senyawa kovalen. Senyawa kovalen terbentuk karena adanya ikatan kovalen yaitu pemakain bersama pasangan elektron atau lebih digunakan bersama - sama oleh kedua atom atau salah satu atom yang berkaitan. Satu atom memberikan satu atau lebih dari elektron.
Apabila senyawanya terionisasi sempurna maka akan dihasilkan larutan elektrolit kuat sedangkan bila senyawanya terionisasi sebagian maka akan dihasilkan larutan elektrolit lemah. Oleh karena ikatan ion dan ikatan kovalen berbeda dalam proses pembentukannya maka senyawa yang dibentuknya juga memiliki sifat-sifat fisika dan kimia yang berbeda. Sebaliknya Senyawa non polar terdiri dari beberapa atom yang memiliki keelektronegatifan yang hampir sama misalnya saja H dan C.
Ikatan Kimia Bentuk Molekul dan Interaksi Antarmolekul. Pada senyawa kovalen di samping itu elektron bersama oleh beberapa atom. Ikatan yang terjadi antara ion-ion logam dan non logam Ikatan terbentuk akibat gaya tarik listrik antara ion yang berbeda Ikatan ion juga dikenal sebagai ikatan elektrovalen.
Dari hasil percobaan yang telah dilakukan dapat diketahui sifat-sifat kimia dan fisika senyawa ion dan senyawa kovalen. Senyawa ion berwujud padatan berbentuk kristal. Hal ini karena air melarutkan zat polar yang merupakan konsistensi senyawa ionik sedangkan senyawa kovalen non-polar.
Anda dapat memprediksi ikatan kovalen akan terbentuk antara dua atom nonlogam. Pada senyawa ionik elektron diberikan dari atom dari satu unsur ke unsur lainnya. Kamu bisa belajar mengenai Gaya Dipol Permanen.
Senyawa ion adalah senyawa yang terbentuk dari ikatan ion sedangkan senyawa kovalen adalah senyawa yang terbentuk dari ikatan kovalen. Ikatan ionik adalah ikatan yang dihasilkan dari perpindahan elektron dari satu atom ke atom lain. Berikut adalah perbedaan daya hantar jenis jenis elektrolit senyawa ion dengan senyawa kovalen polar.
NaCl natrium klorida. Selain senyawa ion ada pula senyawa kovalen. Kesetimbangan Ion dan pH Larutan Garam.
Jelaskan perbedaan antara senyawa kovalen polar dengan kovalen nonpolar. Kepolaran pada molekul ini terjadi karena antara atom H dan atom Cl memiliki perbedaan. Perbedaan antara mereka ada hubungannya dengan seberapa sama atom yang berpartisipasi dalam ikatan berbagi elektron mereka.
INI JAWABAN TERBAIK Perbedaan senyawa ion dan senyawa kovalen. Senyawa polar terbentuk dari ikatan kimia dengan nama ikatan kovalen polar sedangkan senyawa nonpolar terbentuk dari ikatan kovalen nonpolar. Ikatan Ion Ikatan Kovalen Senyawa Polar Non Polar Gaya antar molekul 1.
Jika atom pusat mempunyai pasangan elektron bebas sehingga pasangan elektron berikatan akan tertarik ke salah satu atom maka merupakan senyawa kovalen polar. Ana Daniar Oktavianingrum Indra Lesmana Otniel Victory Febe A Saidatuf Farida 2. Senyawa berikut yang memiliki momen dipol bersifat polar adalah.
Sementara itu lelehan dan larutan senyawa ion dapat menghantarkan listrik. Bentuk padatan bersifat non konduktor karena susunan antar partikel yang rapat sehingga ion-ion tidak dapat bergerak bebas. Jika dibandingkan antara hasil percobaan dengan sifat-sifat kimia dan fisika senyawa ion dan senyawa kovalen pada buru referensi keduanya terdapat kesesuaian.
Senyawa ion larut dalam air dan hanya sebagian yang larut dalam pelarut no polar sedangkan pada senyawa kovalen larut dalam pelarut non polar namun hanya sebagian yang larut dalam air. Kesetimbangan Larutan Ksp Sistem Koloid. Senyawa kovalen polar dalam bentuk larutannya dapat terionisasi sempurna atau terionisasi sebagian menjadi ion-ionnya sehingga dapat menghantarkan arus listrik.
Jika unsur penyusun senyawa kovalen merupakan unsur yang tidak sejenis biasanya merupakan senyawa kovalen polar. Juga senyawa kovalen dapat larut dalam air tetapi tidak berdisosiasi menjadi ion. Meski demikian senyawa kovalen dan ionik memiliki beberapa perbedaan dalam menghantarkan arus listrik.
Senyawa ion larut dalam pelarut polar 3. Senyawa Kovalen Polar dan Non-Polar. Dua jenis ikatan adalah ikatan ion dan ikatan kovalen.
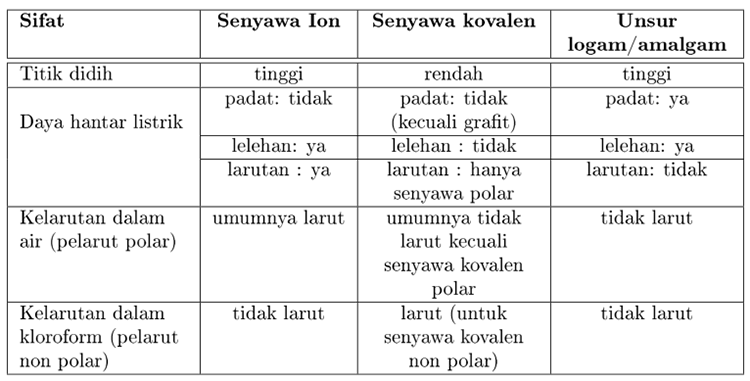
Sifat senyawa ion maupun sifat senyawa kovalen dapat kita jabarkan sebagai berikut.
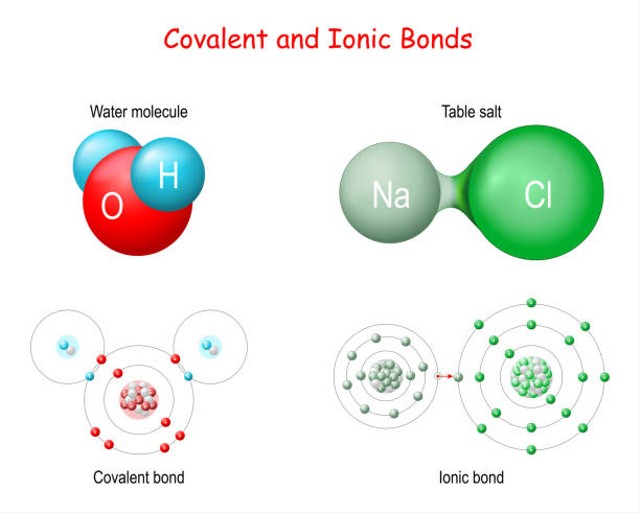
Perbedaan Senyawa Ionik Dan Senyawa Kovalen Polar Kumparan Com

Devised In 1869 The Table Was So Ingenious That It Even Predicted The Elements That Would Fill In Its Ga Periodic Table Chemistry Basics Life Hacks For School

Sifat Senyawa Ion Kovalen Dan Polar Nonpolar Ikatan Kovalen Pdf

1 Senyawa Kovalen Polar Dan Non Polar Ppt Download
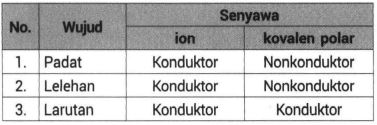
Perbedaan Sifat Senyawa Ion Dan Senyawa Kovalen Po

Kimia Kelas X Ikatan Kovalen Polar Non Polar Senyawa Kovalen Polar Dan Senyawa Kovalen Nonpolar Youtube

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection

Perbedaan Senyawa Ion Dan Senyawa Kovalen Youtube

Ciri Ciri Ikatan Ion Ikatan Kovalen Polar Dan Nonpolar Brainly Co Id

Perbedaan Utama Senyawa Kovalen Polar Dengan Senyawa Ionik Adalah

Sifat Senyawa Ion Dan Senyawa Kovalen Ikatan Kimia Youtube

Ikatan Kovalen Non Polar Kovalen Polar Dan Kovalen Semi Polar Youtube

Bandingkan Sifat Senyawa Ionik Dan Senyawa Kovalen
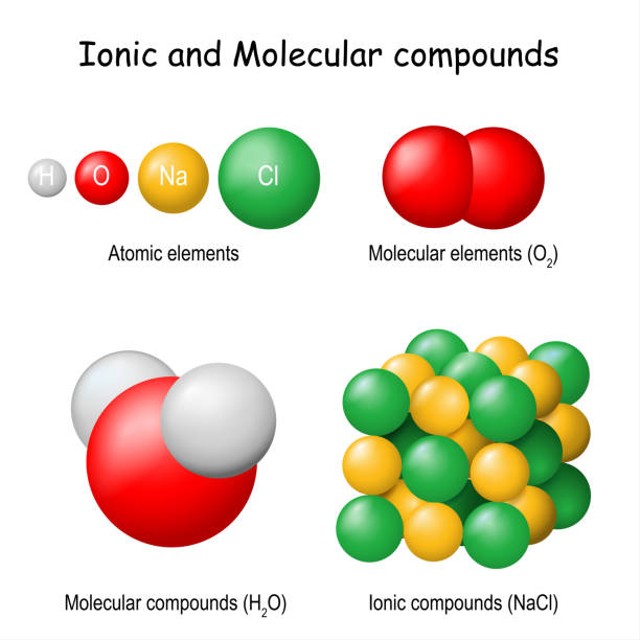
Perbedaan Senyawa Ionik Dan Senyawa Kovalen Polar Kumparan Com

Pengertian Senyawa Kovalen Polar Dan Nonpolar Serta Perbedaannya
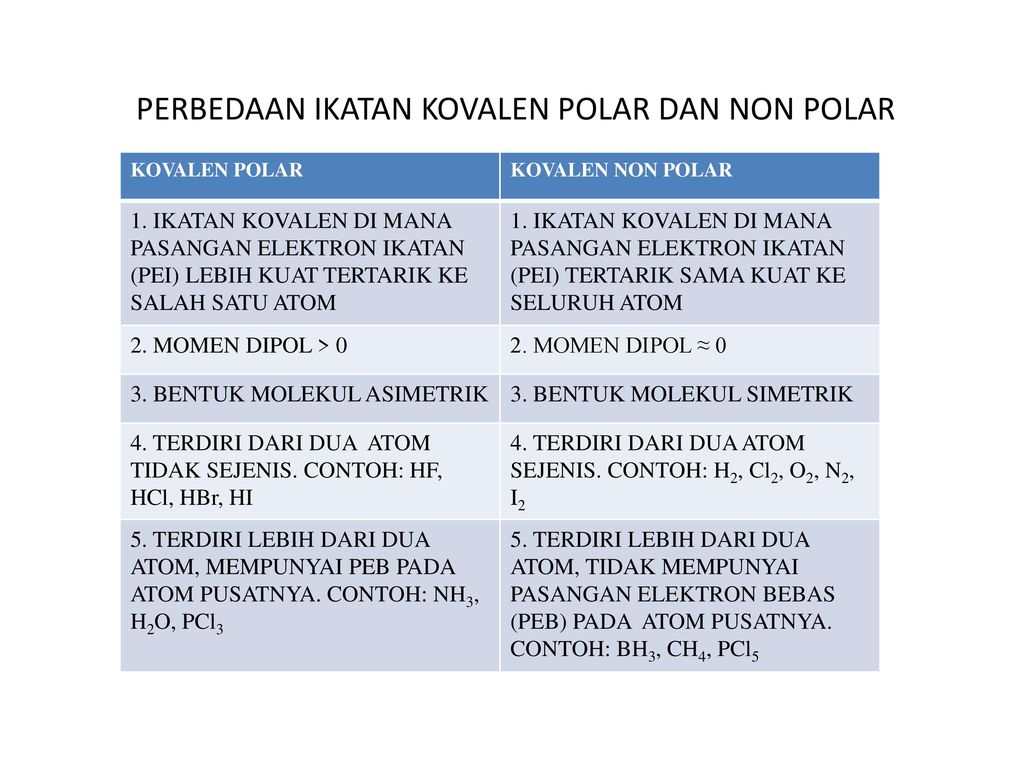
Perbedaan Ikatan Kovalen Polar Dan Non Polar Ppt Download

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection
Modul Rumus Soal Sifat Fisis Senyawa Wardaya College

Perbedaan Senyawa Ion Senyawa Kovalen Dan Lo Utakatikotak Com

